Методы обучения химии. Ученые об «Основах химии Как понять химию с нуля за день
Всем известно, что школьный курс является той основой, которая дает самые необходимые знания о мире, в котором мы живем. Это действительно так и такой предмет как химия прекрасное тому подтверждение, так как, по сути, абсолютно все, что нас окружает и есть химия — химические элементы, их соединения, процессы взаимодействия и т.д. Поэтому неудивительно, что в школьный курс входит много тем по химии .
Важность изучения химии
Изучая предмет химии, школьник не только познает мир и определенные законы его существования, но и развивает память, логическое и абстрактное мышление, аналитические способности и интеллектуальные возможности в целом. ЕГЭ по химии, который является предметом по выбору, есть ни что иное как закономерное подведение итогов учебно-образовательной деятельности.
Кроме того, успешная сдача ЕГЭ по химии после окончания школы облегчит получение высшего образования, ведь его результаты высшими учебными заведениями засчитываются как вступительные экзамены. Поэтому нужно относиться к этому экзамену как к важному этапу в вашем будущем. Благодаря полученным знаниям будет проще потом осваивать другие сложные предметы в университете.
Что представляет собой подготовка к ЕГЭ по химии
Конечно, залогом успешного изучения и усвоения материала является постоянная работа — это касается абсолютно всех предметов. Однако такой специфический предмет как химия, зачастую требует особого подхода и применения дополнительных методов обучения. Например, таковыми являются самостоятельная работа или систематические занятия с репетитором. Но что делать, когда возможности для дополнительных занятий с преподавателем нет, а некоторые разобрать по учебнику практически не реально, впрочем, как и систематизировать все полученные знания, когда это необходимо для подготовки к ЕГЭ по химии?
Сегодня существует прекрасная возможность для дополнительного образования, расширения, углубления знаний и закрепления пройденных материалов — химия онлайн бесплатно. Такие уроки основаны на многолетнем педагогическо-психологическом опыте. Всемирная сеть в этом случае становится надежным другом и помощником современной молодежи, предлагая изучение различных тем по химии, включая различные методы подачи материала — видеоуроки с пояснениями, примерами опытов, решением практических задач и многое другое, систематизированные оптимальным образом электронные конспекты и таблицы.
Эта наука столь сложна, сколь и интересна. Однако уроки химии онлайн позволяют наиболее эффективно усвоить даже самую сложную тему, а при необходимости — проконсультироваться с квалифицированным преподавателем, в том числе и по вопросам, касающимся ЕГЭ по химии. Все это делает обучение легким и понятным, каждый может избежать сложных вопросов, разобраться в темах, которые пропустил ранее.
Итого
Занимаясь химией онлайн и бесплатно , вы в доступной для усвоения форме перенимаете многолетний опыт и получаете багаж систематизированных знаний. Каждый может выбрать для себя различные режимы и варианты обучения. Выпускники могут повторять пройденный в школе материал и восполнять имеющиеся пробелы в знаниях, выполняя задания различной сложности и изучая темы по химии по той системе, на которой и основан ЕГЭ. Конечно, готовых ответов никто не предоставит, тем более что каждый год список вопросов и заданий меняется. Однако структура в основном остается прежней, позволяя разработчикам совершенствовать эффективность оценки, а учащимся — наиболее полно раскрывать свой потенциал. Возможно, это поможет и школам показывать лучшую успеваемость своих учеников.
Кроме того, уроки химии онлайн — это удобно, а также может пригодиться как практикующим преподавателям для перенятия опыта, так и родителям, для того чтобы быть в курсе того, как сегодня строится процесс обучения их детей. Занятия химией онлайн помогут освежить знания будущим абитуриентам, желающим получить еще одно образование. Поэтому трудно поспорить с тем, что благодаря возможностям Интернета учиться становится проще абсолютно всем.
Значение «Основ химии»
Университет был центром жизни Д. И. Менделеева, местом, где он передавал слушателям свои неисчерпаемые знания. Целые поколения химиков являются учениками Д. И. Менделеева -- не только те, кто слушал его лекции непосредственно в стенах университета и в других высших учебных заведениях, а и все те, кто изучал химию по его «Основам химии».
«Основы химии были написаны Д.И. Менделеевым вскоре после того, как он начал читать курс неорганической химии в университете. Д.И. Менделеев отмечал: «Писать начал, когда стал после Воскресенского читать неорганическую химию в университете и когда, перебрав все книги, не нашел, что следует рекомендовать студентам...»
Этот труд и поныне является настольной книгой каждого образованного химика как энциклопедия химии. «Эти «Основы»,-- говорил Д. И. Менделеев,-- любимое дитя мое. В них мой образ, мой опыт педагога и мои задушевные научные мысли...»
В «Основах химии» сочетается глубокая научность изложения предмета с раскрытием основных методологических установок или, как говорил Д. И. Менделеев, «философского направления», тесная и неразрывная связь теории и практики и исторический подход к освещению ряда вопросов. Автор считал, что надо «уважать историю» и овладеть культурным наследием прошлого, без чего невозможно идти вперед. Наконец, в этой книге с присущей Д. И. Менделееву последовательностью, ясностью и отчетливостью дается определение основных химических понятий и слов, показывается значение химического эксперимента и методики работа над книгой.
«Основы химии» не просто учат, а приучают к труду. Д. И. Менделеев в предисловии к «Основам химии» писал: «Я старался развить в читателе дух пытливости, не довольствующийся простым описанием или созерцанием, а возбуждающий и приучающий к упорному труду и стремящийся везде, где можно, мысли проверять опытами».
Огромную роль сыграли "Основы химии" в развитии отечественного химического образования. При жизни Менделеева они издавались восемь раз. Первое издание в 4-х выпусках увидело свет в 1868 - 1871 гг., восьмое -- в 1905-1906 гг. Еще пять раз книга переиздавалась в советский период.
Тысячи ученых, инженеров и других специалистов учились по этой книге, в том числе ученики и последователи Д. И. Менделеева: А. А. Банков, В. И. Вернадский, Г. Г. Густавсон, В. Л. Комаров, К. А. Тимирязев, В. Е. Тищенко и другие. Этот образцовый учебник Менделеева был переведен на английский, французский и немецкий языки.
Ученые об «Основах химии»
«Основы химии» - классическое произведение Д.И. Менделеева содержащее изложение неорганической химии с точки зрения периодического закона химических элементов. В этой книге неорганическая химия - наука о химических элементах и образуемых ими соединениях - благодаря периодическому закону, открытому Д.И. Менделеевым в 1869 г. в связи с поисками им общего признака классификации химических элементов, впервые предстала как стройное научное здание, а не беспорядочное накопление отдельных фактов. По богатству и смелости научных идей, по оригинальности освещения фактов, по влиянию, которое они оказали на развитие химии и на ее преподавание, «Основы химии» являются единственным в своем роде трудом в мировой химической литературе.
Теплых высказываний как о Менделееве, так и о его книге «Основы химии» в литературе много.
Известный физико-химик и металловед академик А.А. Байков говорил: «Можно сказать, что химия как наука стала существовать только после Менделеева. До Менделеева были отдельные разрозненные химические знания, но не было химии как отдельной науки, в которой ее многообразное и разнообразное содержание было бы объединено и связано в стройную цельную систему. Эту задачу и выполнил Менделеев, и эта задача получила свое воплощение в том замечательном труде его, который называется «Основы химии» и в котором заключается полное изложение периодического закона». Далее он указывал: «Основы химии представляют собой систематическое изложение всей химии, и периодический закон является средством для того, чтобы разобраться в бесконечном разнообразии отдельных фактов и явлений, из которых слагается химическая наука, и привести их в стройную органически цельную систему. Периодический закон неотделим от «Основ химии».
О значении «Основ химии» Д.И. Менделеева говорят в наши дни слова академика Б. М. Кедрова и В. А. Волкова, высказанные ими в печати в 1982 г.: «Химию можно определить как учение об элементах и их соединениях». Такое определение предмета химии впервые дал
Д.И. Менделеев в 1871 г. в своих «Основах химии».
Предоставим слово одному из основоположников геохимии академику В.И. Вернадскому: «В «Основах химии» проблемы геохимии и космической химии получали не только яркое освещение, но нередко выступали на первое место. Как всегда у Д.И. Менделеева, это не было повторением того, что давалось другими, - на каждом шагу встречается новое, найденное его яркой личностью, схваченное его всеобъемлющим умом».
А теперь возвратимся еще раз к словам А. А. Байкова: «Основы химии» Менделеева, воплотившие в себе периодический закон, - это памятник, который по силе своего замысла, по совершенству исполнения и глубине мысли является таким же величайшим проявлением человеческого гения, как «Божественная комедия», Данте, как «Страшный суд» Микеланджело, как 9-я симфония Бетховена».
«Основы химии» объединяли всех русских химиков, были связующим звеном между ними Дмитрием Ивановичем, а потому все мы являемся его учениками, преданными и его научным заветам...», - так говорил академик Н.Д. Зелинский.
В 1907 г. английский химик Т. П. Торп об «Основах химии» Д.И. Менделеева писал: «Благодаря своему проникновению, умению схватывать детали и принципы, вызывать на размышления, благодаря необычайной силе координации и богатству мыслей - это книга из книг, которая может быть прочитана каждым студентом, независимо от возраста, с пользой и удовлетворением, окрашенным иногда некоторой долей занимательности. Тем, кому посчастливилось лично знать автора, каждая страница напоминает о его личности. Даже подстрочные примечания носят характер индивидуальности и оригинальности. Можно сказать, что менделеевские «Основы» имеют такое же значение для химической науки второй половины девятнадцатого века, как и «Новая система» Дальтона для первой половины этого столетия... Благодаря его способности широко и всеобъемлюще мысленно охватывать химические процессы, Менделеев заслужил звание философа химической науки».
Нас восхищают слова итальянского ученого и историка химии М. Джуа: «Еще в то время, когда я в юношеские годы обратился к изучению химии, привлеченный в Римский университет преподаванием Каниццаро, передо мной предстала в полном блеске фигура Д. И. Менделеева, и не только благодаря созданию им периодической системы элементов, но и как автора «Основ химии», книги, которая стала доступна итальянским ученым благодаря переводам Л. Явейна и А. Тилло на немецкий и Г. Каменского на английский язык».
Академик Д. П. Коновалов был учеником Д. И. Менделеева сменившим своего учителя на кафедре химии Петербургского университета. Для 9-го издания «Основ химии», которое было выпущено к 20-летию со дня смерти Д. И. Менделеева, Коновалов подготовил статью «Основы химии» и их автор», в которой на основе анализа трудов Д.И. Менделеева и своих личных воспоминаний и дал сжатый, но содержательный обзор основных направлений научной деятельности Д.И. Менделеева.
Академик Б.М. Кедров пишет: «На примере Менделеева можно видеть, что открытию периодического закона предшествовал гигантский труд, вложенный их в изучение всего, что касалось химических элементов. Этот труд занял пятнадцать лет ежедневных, ежечасных размышлений, лабораторных исследований, чтения бесчисленных статей и книг по химии. Все это воплощалось Менделеевым в его публикациях, лекциях, докладах и особенно в его «Основах химии».
Высказывания известных людей об «Основах химии» Д.И. Менделеева могли 6ы быть продолжены. Мы их заканчиваем, обращаясь еще раз к словам академика А.А. Байкова: «Для всех нас смерть Д.И. Менделеева была потрясающим событием. Одно для нас являлось утешением, - то, что его жизнь не прошла бесследно, что он оставил нам богатейшее наследство, и в этом наследстве наиболее крупным памятником являются его труды, связанные с периодическим законом и «Основами химии». И поскольку в «Основах химии» воплотился периодический закон, «Основы химии» являются тем памятником, который по грандиозности своего содержания, по величеству замысла, по совершенству выполнения и глубине мысли является величайшим проявлением человеческого гения».
I.Я хочу научиться находить относительную молекулярную массу .Прекрасно! Начинаем учиться. предположим, нам надо найти относительную молекулярную массу сульфата натрия Na 2 SO 4 ,наши действия:
1. Нашли в Периодической системе натрий (№11)
2.Увидели под названием число 22,9 и округлили до 23.
3. Так как атомов натрия два, мы умножим 23 на 2 и получим 46.
4. Нашли в периодической системе серу (№16)
5. Увидели под названием число 32, умножать не будем, т.к. атомов серы один.
6.
Нашли в Периодической системе кислород (№8)
7.Под названием написано 15,9, округляем, получаем 16. Атомов
кислорода в молекуле 4, значит нам надо умножить 16 на 4. Получаем 64.
8 Последнее действие:
46+32+64=142 Ура! мы нашли относительную молекулярную массу сульфата натрия.
Пожалуй, вам стоит поупражняться самостоятельно.
Попробуйте посчитать для:
H 2 SO 4 у вас должно получиться 98
Ca(OH) 2 у вас должно получиться 74
K3PO4 у вас должно получиться 212
Если вы справились, то примите наши поздравления. Вы сделали первый шаг в решении задач.
Напоминаем, что молярная масса численно равна молекулярной, но измеряется в граммах/на моль(г/моль).
II.Я хочу научиться находить количество молей вещества.
Вам потребуются формулы:
n=m /M используем, если нам дана масса
n=v /V M используем, если нам дан объём
n=N/ N A используем, если нам дано количество атомов или молекул .
Задача: найти количество вещества сульфата натрия массой 7,1г.
Дано: решение:
m(Na 2 SO 4)=7,1 г Нам дана масса, значит мы будем использовать формулу с массой
_____________ n=m / M, где М- молярная масса
(если мы не умеем её считать, см.п.I)
Найти: n M((Na 2 SO 4) =46+32+16*4=142 г/моль
n= 7,1г / 142г/моль= 0,05 моль
Ответ: n=0,05 моль
Попробуйте самостоятельно найти количество вещества, если дано
1. 196г H 2 SO 4
(ответ 2 моль)
2.20,2г KNO 3 (ответ 0,2 моль)
3. 16г NaOH (ответ 0,4 моль)
Предлагаем вам самостоятельно решить следующие задачи: (не бойтесь, вы справитесь!)
1. Найдите количество вещества, которое составляеют 49г гидроксида меди (II).
2.Сколько молекул содержат 4,48л водорода?
3.
Найдите массу 5,6л азота.
4. Какой объём занимает оксидсеры (IV) массой 80г?
Решение этих задач покажите своему учителю химии. Задайте вопросы, если что-то непонятно.
III. Я хочу научиться решать задачи с расчетом по уравненению реакции.
Задача: найдите массу оксида магния, который может раствориться в 12,6г азотной кислоты.
Дано:
m(HNO 3)=12.6г
___________
Найти:m(MgO)
Решение: 1
. Первое действие любой подобной задачи - найти количество молей данного вещества
.
для этого мы пользуемся формулой (см.п.2).Так как нам дана масса,
наша формула: n=m / M
n(HNO 3)= 12.6г /M(HNO 3)=12.6 / (1+14+48) =12.6 / 63 =0.2 моль
2.
Второе действие - записать уравнение реакции, расставить коэффициенты.
3.
Третье действие - надписать количество молей
, вычисленное в первом действии, над веществом, для которого оно вычислено, а над искомым поставить х
х
,,,0.2 моль
MgO +2 HNO 3 = Mg(NO 3) 2 + H 2 O
4.
Под этими веществами
записать количество вещества, нужное по уравнению - коэффициент реакции:
х............0.2 моль
MgO +
2
HNO 3 = Mg(NO 3) 2 + H 2 O
1 моль
2 моль
5. Таким образом у нас получилась запись
х............0.2 моль
MgO +2 HNO 3 = Mg(NO 3) 2 + H 2 O
1 моль 2 моль
В этой записи увидим пропорцию: х:1 =0.2: 2 ,
решаем уравнение
(произведение крайних членов пропорции равно произведению средних) х= 0.1, то есть n(MgO
)=0.1моль
5.
Мы нашли количество вещества, а нас спрашивают массу. Используем формулу:
m=n*M
m(
MgO
)=0.1*(24+16) =4г
Ответ: масса оксида магния 4г.
Попробуйте самостоятельно решит задачи: ( Будьте внимательны и аккуратны!)
1.
Вычислите объём оксида серы (IV), который образуется при горении 80г серы.
2. Вычислите массу оксида алюминия, который образуется при горении алюминия в 4,48л кислорода
.
3. Найти объём кислорода, который необходим для сжигания 12г магния.
4.
Найти массу оксида цинка, который образуется при взаимодействии цинка с 11,2л кислорода.
5.
Найти массу оксида натрия, который образуется при взаимодействии натрия с 4,48л кислорода.
6.
Найти объём углекислого газа, который образуется при горении 60г угля.
7.
Найти объём кислорода, который расходуется при горении 3,1г фосфора.
8.
Найти массу фосфора, который может сгореть в 4,48л кислорода.
9.
Найти объём хлора, который необходим для взаимодействия с 5,4г алюминия.
10. Найти объём хлора, с которым могут прореагировать 4,6г натрия.
11.
Найти массу хлорида алюминия, который образуется при взаимодействии с алюминием 1,12л хлора.
12. Найти массу хлорида железа (III), который образуется при взаимодействии с железом 11,2л хлора.
13. Сколько литров кислорода потребуется для сжигания 6,2г фосфора?
14.
Найти массу оксида углерода (IV), который образуется при горении угля в 8,96л кислорода.
IV. Я хочу научиться записывать схему электронной конфигурации атома (электронный паспорт)
Для этого вам необходимо запомнить, что на s-орбитали может
находиться не более 2 электронов, на р- орбитали - не более шести, на d-
орбитали не более 10, на f- орбитали - не более 14.
итак:
S - 2
P - 6
d - 10
f
- 14
Заполнение электронами орбиталей происходит в следующем порядке:
1s2s
2p
3s
3p
4s
3d
4p
5s
4d
5p
6s
4f5d
6p
7s
5f6d
7p
Обратите внимание, что номер d-орбитали всегда на один меньше, чем номер s-орбитали, после которой она расположена.
Количество электронов в атоме равно количеству протонов в его ядре, равно номеру элемента в Периодической системе.
Итак, предположем, что нам надо составить схему электронной конфигурации атома калия.
Его номер 19, значит в атоме 19 электронов.
Начинаем по порядку с 1s, заполня орбитали максимально возможным
для них количеством электронов и записывая это количество как степень
над символом орбитали:
1s 2 2s 2 2p 6 3s 2 3p 6 4s 1
На последней орбитали оказывается один электрон, т.к. нам надо "пристроить" всего 19 электронов и записав1s 2 2s 2 2p 6 3s 2 3p 6 у нас остается как раз один электрон. Он и будет располагаться на следующей по порядку орбитали 4s.
Проверим себя:
Калий находится в четвертом периоде
следовательно внешний уровень четвертый.
Калий находится в первой группе,
следовательно на внешнем уровне у него один электрон.
Мы написали схему правильно.
Нам требуется потренироваться.
Попробуйте написать электронные паспорта для атомов хлора,
натрия, азота, магния, кислорода. А потом замахнитесь на вольфрам,
сурьму, йод, барий и т.д. У вас получится, надо толко быть акккуратным и
настойчивым.
Проверьте себя:
Cl 1s 2 2s 2 2p 6 3s 2 3p 5
Na 1s 2 2s 2 2p 6 3s 1
N 1s 2 2s 2 2p 3
Mg 1s 2 2s 2 2p 6 3s 2
O 1s 2 2s 2 2p 4
V
Я хочу научиться пердсказывать свойства элемента по положению в Периодической системе.
Наиболее энергетически выгодно состояние с заполненным внешним уровнем (8 электронов
). Такую конфигурацию имеют элементы неон, аргон, криптон, ксенон и радон
. они называются инертные)благородные) газы, так как не вступают во взаимодействие. Они расположены в 8-ой группе.
Остальные элементы
или
присоединяют
недостающие до 8 электроны
например Cl на внешнем уровне 7 электронов(напишите его паспорт)
,
не хватает 1 будет присоединять 1 электрон.
например О на внешнем уровне 6 электронов(напишите его паспорт)
, не хватает 2, будет присоединять 2 электрона.
присоединять электроны будут элементы, имеющие на внешенем уровне 4-7 электронов. Такие элементы называются НЕМЕТАЛЛЫ. Чем легче элемент присоединяет электроны, тем он более активный неметалл.
Посмотрите в Периодическую систему и объясните, почему проявляют неметаллические свойства фосфор, мышьяк, селен, бром, азот, фтор, углерод.
или
отдают
электроны с внешнего уровня, в результате чего внешним становится заполненный предыдущий уровень.
например натрий имеет на внешнем уровне 1 электрон, а на предыдущем 8, (напишите его паспорт)
, поэтому натрий отдаёт 1электрон.
например алюминий имеет на внешнем уровне 3 электрона, а на предыдущем 8( напишите его паспорт),
поэтому алюминий отдаёт 3 электрона.
Отдавать электроны будут элементы, имеющие на внешнем уровне 1-3 электрона. Это МЕТАЛЛЫ. Чем легче элемент отдаёт электорны, тем он более активный металл.
Найдите в Периодической системе магний, калий, индий, рубидий, кальций
и объясните их свойства.
Способность брать или отдавать электроны зависит и от расстояния между ядром и внешним уровнем
, которое определяет силу притяжения электронов внешего уровня к ядру.
например, азот и висмут расположены в V группе, значит у них 5
электронов на внешнем уровне и они оба должны быть неметаллами. Но висмут - металл
, так как его внешний уровень
(6-ой, мы это узнали по номеру периода
) расположен далеко от ядра,
притяжение
электоронов внешнего уровня к ядру небольшое
и висмут не присоединяет электроны, а отдает
, поэтому и металл.
Сравните свойства углерода и олова, серы и полония.
Используя "волшебные слова" - расстояние и притяжение
, - объясните свой вывод.
Я хочу научиться распозновать основные классы неорганических веществ и знать их свойства.
Существует 4 основных класса веществ:
оксиды
, кислоты,
основания
и соли.
Вам необходимо выучить определения:
оксиды
- сложные вещества, состоящие из двух элементов, один из которых кислород.
оксид
- ЭхОу
например: Na 2 O - оксид натрия, CuO - оксид меди(II), P 2 O 5 -оксид фосфора
кислоты
- сложные вещества, состоящие из атомов водорода и кислотноо остатка.
кислота - НхА,
где А- кислотный остаток.
например HCl- соляная кислота, H 2 SO 4 - серная кислота, HNO 3 - азотная кислота
основания - сложные вещества, состоящие из атомов металла и гидроксогрупп ОН.
основание - Ме(ОН)х
например: КОН - гидроксид калия, Са(ОН) 2 - гидроксид кальция

соли - сложные вещества, состоящие из атомов металла и кислотного остатка.
соль- МехАу
например: Na 2 SO 4 - сульфат натрия, Cu(NO 3) 2 - нитрат меди (II).
Проверим, как вы поняли классификацию.
В каждой строчке найдите лишнее вещество:
1. NaOH HCl Mg(OH) 2 Fe(OH) 3
2. HNO 3 H 2 SO 4 H 2 O HCl
3. Cl 2 O 7 MnO NaOH K 2 O
4. Ca(OH) 2 CuCl 2 Na 2 SO 3 Mn(NO 3) 2
5.
CuSO 4 NaCl FeCO 3 H 3 PO 4
проверьте свои ответы:
1. HCl - это кислота, а все остальные вещества - основания
2. Н 2 O - это оксид, а все остальные вещества - кислоты.
3. NaOH - это основание, а все остальные вещества - оксиды.
4. Са(ОН) 2
-это основание, а все остальные вещества - соли.
5. H 3 PO 4 - это кислота, а все остальные вещества - соли.
Теперь стоит заняться химическими свойствами.
Свойства оксидов зависят от того, какой элемент образует оксид.
если элемент - металл
, то в большинстве случаев он образует основной оксид
,
если эемент - неметалл
, то его оксид, в боольшинстве случаев, кислотный.
основной оксид + вода = щелочь (растворимое основание) 1
+ кислота = соль и вода 2
+кислотный оксид = соль 3
Запомните эту схему! Она нам очень пригодится. Как же эта схема поможет нам написать уравнения реакций?
Например:
вам нужно закончить уравнение и расставить коэффициенты:
СаО + НNO 3 =
Ваши действия:
1. Выяснить, что за вещества реагируют:
СаО - оксид, оксид металла, значит основной оксид
НNO 3 - кислота
2.
определить номер свойства
основной оксид + кислота - свойство №2, значит должны получиться соль и вода
3. Что такое соль? (Это сложное вещество, состоящее из атомов металла и кислотного остатка)
кто здесь металл? (кальций
)
Где кислотный остаток?(он входит в состав кислоты, этo NO 3)
4. Чтобы правильно записать формулу соли, нужно учесть валентность (у кальция - II, у кислотного остатка - 1).
Пишем уравнение:
CaO +HNO 3 = Ca(NO 3) 2 + H 2 O
5. Ставим коэффициенты:
CaO +2 HNO 3 = Ca(NO 3) 2 + H 2 O
А теперь попробуйте самостоятельно закончить уравнения реакций и расставить коэффициенты:
MgO+HCl=
Na 2 O +H 3 PO 4 =
CuO + H 2 SO 4 =
BaO + H 2 O =
Na 2 O +H 2 O =
CaO + CO 2 =
MgO + P 2 O 5 =
Если захотите проверить результат, покажите то, что у вас получилось Александре Евгеньевне. Она с удовольствием проверит, объяснит ошибки, а если их не будет, поставит "5" в журнал.
Давайте теперь рассмотрим свойства кислотных оксидов.
кислотный оксид + вода = кислота 4
+ щелочь = соль + вода 5
+ основной оксид = соль 6
Допустим, нам надо закончить следующее уравнение и расставить коэффициенты:
P 2 O 5 +H 2 O =
Наши рассуждения:
1. К какому классу веществ относится первое вещество? (оксид, оксид неметалла, кислотный оксид).
2. Определяем номер свойства
(кислотный оксид +вода это свойство №4, должна получиться кислота.)
3. Что такое кислота?(
сложное вещество,состоящее из атомов водорода и кислотного остатка)
4. Записываем уравнение:
P 2 O 5 +H 2 O =
H 3 PO 4
Расставляем коэффициенты:
P 2 O 5 +3H 2 O =
2H 3 PO 4
А теперь попробуйте самостоятельно:
CO 2 +H 2 O=
SiO 2 + KOH =
P 2 O 5 + LiOH =
CO 2 +Ca(OH) 2 =
SO 3 + MgO =
Если вы хотите проверить свою работу, покажите её Александе Евгеньевне.
Рассмотрим свойства кислот.
кислота + металл(стоящий в ряду напряжений до водорода
) = соль + Н 2
+ оксид металла = соль + вода
+ основание = соль + вода
+ соль = другая соль + другая кислота ( в этой реакции должен образоваться осадок или выделиться газ
)
Попробуем потренироваться в выборе веществ, способных реагировать с кислотами.
С каким веществом может реагировать соляная кислота?
Медь стоит в ряду напряжений после водорода, поэтому не реагирует с раствором соляной кислоты.
Оксид серы - это кислотный оксид, так как сера - неметалл. С кислотными оксидами кислоты не реагируют.
Вы сделали правильный выбор. Гидроксид магния - это основание. Кислоты взаимодействуют с основаниями с образованием соли и воды.
C неметаллами, коим является кислород, кислоты не взаимодействуют.
А теперь работаем самостоятельно.
В каждой строчке найдите вещество, способное взаимодействовать с раствором серной кислоты.
Ag CuO HNO 3 NaCl
Mg(OH) 2 KCl Hg CO 2
P P 2 O 5 K 3 PO 4 K 2 O
Li 2 SO 4 LiCl LiNO 3 Li 2 CO 3
Ответы: CuO . Mg(OH) 2 . K 2 O. Li 2 CO 3
ЗАПОМНИТЕ:
Все карбонаты реагируют с кислотами, так как в результате
образуется нестойкая угольная кислота, которая сразу же разлагается на
углекислый газ и воду:
H 2 CO 3 = CO 2 + H 2 O
Закончите уравнения реакций, расставьте коэффициенты:
HNO 3 + Ca(OH) 2 =
HNO 3 + MgO =
HNO 3 + К 2 CO 3 =
H 3 PO 4
+ KOH =
H 3 PO 4
+ BaO
=
H 3 PO 4
+ Na 2 SiO 3 =
Рассмотрим свойства оснований.
Растворимые и нерастворимые основания отличаются по свойствам.
щелочь + кислота = соль + вода
(растворимое основание)
+Кислотный оксид = соль +вода
+соль= другая соль + другое основание
( должен выпасть осадок)
Закончи
те уравнения реакций, расставьте коэффициенты
:
Ca(OH) 2
+ CuCl 2
Ca(OH) 2
+ Al(NO 3) 3
Ca(OH) 2
+ ZnSO 4
неравтворимое основание + кислота = соль +вода
при нагревании разлагается = оксид + вода
Закончите уравнения реакций, поставьте коэффициенты:
Cu(OH) 2
+ HCl
Zn(OH) 2
+ H
NO 3
Cu(OH) 2
=
Рассмотрим свойства солей:
Соль + кислота = другая соль +другая кислота
+ щелочь = другая соль + другое основание
+ соль = другая соль + другая соль
+ более активный металл = другая соль + другой металл
(в первых трех реакциях должен выпасть осадок)
Закончите уравнения возможных
реакций, расставьте коэффициенты, укажите вещество, выпадающее в осадок:
ZnSO 4
+KOH
=
ZnSO 4
+K 3 PO 4 =
ZnSO 4 +HNO 3 =
Al(NO 3) 3 +
HCl
=
Al(NO 3) 3 +
P 2 O 5
=
Al(NO 3) 3 +
Cа(OH) 2
=
CuCl 2
+ Mg=
CuCl 2
+ Hg =
Учите, дети, химию!

Прекрасно! В ионных уравнениях нет ничего сложного. От вас потребуется внимательность и аккуратность, ну и, конечно, знание свойств основных классов соединений, о чем уже рассказано выше.
Запомните: На ионы не диссоциируют оксиды, вода и нерастворимыен вещества.
Приступим. Предположим у нас есть уравнение
Mg(OH) 2 +2HCl = MgCl 2 + 2H 2 O
Теперь нам нужно рассмотреть возможность диссоциации каждого из записанных веществ и составить ионное уравнение. Смотрим в таблицу растворимость и ищем Mg(OH) 2 . Видим, что он нерастворим. Это значит, что просто переписываем его
Mg(OH) 2 +и идем дальше.Ищем в таблице растворимости HCl . Видим, что это вещество растворимо. Прекрасно! Мы пишем те ионы, которые написаны в таблице:
Mg(OH) 2 +Н + + Cl - , но в уравнении перед НСl был коеффициент 2, значит у нас 2Н + и 2 Сl -
Mg(OH) 2 +2Н + + 2Cl -
Но в формуле после хлора был индекс 2. Значит у нас 2 хлора. Значит в уравнении перед ионом хлора мы поставим 2.
Mg(OH) 2 +2Н + + 2Cl - =Мg 2+ +2 Cl -
Теперь вода. Но мы помним: вода не диссоциирует, переписываем как есть.
Mg(OH) 2 +2Н + + 2Cl - =Мg 2+ +2 Cl - + 2H 2 O
Мы записали полное ионное уравнение. УРА! Теперь надо найти одинаковые ионы в левой и правой части уравнения и сократить их, как в алгебраическом уравнении.
Mg(OH) 2 +2Н + + 2Cl - =Мg 2+ +2 Cl - + 2H 2 O
Переписываем без них
Mg(OH) 2 +2Н + =Мg 2+ + 2H 2 O
У нас получилось сокращенное ионное уравнение. В результате наша запись выглядит так:
Mg(OH) 2 +2HCl = MgCl 2 + 2H 2 O
Mg(OH) 2 +2Н + + 2Cl - =Мg 2+ +2 Cl - + 2H 2 O
Mg(OH) 2 +2Н + =Мg 2+ + 2H 2 O
Поздравляю. Это ваше первое ионное уравнение. Надеюсь, не последнее. Нужно потренироваться. Сначала воспользуйтесь уже готовыми уравнениями:
2HNO 3 + Ca(OH) 2 =Ca(NO 3) 2 + 2H 2 O
2HNO 3 + MgO =Mg(NO 3) 2 + H 2 O
2HNO 3 + К 2 CO 3 = 2KNO 3 + CO 2 + H 2 O Угольная кислота не существует!
Проверьте себя, найдите ошибки
2HNO 3 + Ca(OH) 2 =Ca(NO 3) 2 + 2H 2 O
2H + +2NO 3 - + Ca 2+ +2OH - =Ca 2+ +2NO 3 - + 2H 2 O
2H + +2OH - = 2H 2 O
2HNO 3 + MgO =Mg(NO 3) 2 + H 2 O
2H + +2NO 3 - + MgO =Mg 2+ +2NO 3 - + H 2 O
2H + + MgO =Mg 2+ + H 2 O
2HNO 3 + К 2 CO 3 = 2KNO 3 + CO 2 + H 2 O
2H + +2NO 3 - + 2 К + +CO 3 2- = 2K + + 2NO 3 - + CO 2 + H 2 O
2H + +CO 3 2- = CO 2 + H 2 O
Надеюсь, что ошибок было немного.
Потренируйтксь еще. Закончите уравнения реакций, расставьте коеффициенты, запишите ионные уравнения:
ZnSO 4 +
Предсказание свойств элемента по положению в Периодической систем е
сновные классы неорганических веществ
Ионные уравнения реакций
Е.Н.ФРЕНКЕЛЬ
Самоучитель по химии
Пособие для тех, кто не знает, но хочет узнать и понять химию
Часть I. Элементы общей химии
(первый уровень сложности)
Я, Френкель Евгения Николаевна, заслуженный работник высшей школы РФ, выпускница химического факультета МГУ 1972 г., педагогический стаж 34 года. Кроме того, я мать троих детей и бабушка четырех внуков, старший из которых школьник.
Меня волнует проблема школьных учебников. Главная беда многих из них – тяжелый язык, который требует дополнительного «перевода» на понятный школьнику язык изложения учебного материала. Ко мне часто обращаются ученики средней школы с такой просьбой: «Переведите текст учебника, чтобы понятно было». Поэтому я написала «Самоучитель по химии», в котором многие сложные вопросы изложены вполне доступно и в то же время научно. На основе этого «Самоучителя», который был написан в 1991 г., я разработала программу и содержание подготовительных курсов. На них обучались сотни школьников. Многие из них начинали с нуля и за 40 занятий понимали предмет настолько, что сдавали экзамены на «4» и «5». Поэтому в нашем городе мои пособия-самоучители расходятся как горячие пирожки.
Может, и другим пригодятся мои наработки?
Статья подготовлена при поддержке учебного центра «МакарОФФ». Учебный центр предлагает Вам пройти курсы маникюра в Москве недорого . Профессиональная школа маникюра проводит обучение по маникюру, педикюру, наращиванию и дизайну ногтей, а также курсы мастеров-универсалов ногтевого сервиса, наращивание ресниц, микроблейдинг, шугаринг и эпиляция воском. Центр выдаёт дипломы после обучения и гарантированное трудоустройство. Подробная информация обо всех программах обучения, цены, расписание, акции и скидки, контакты на сайте: www.akademiyauspeha.ru .
Предисловие
Уважаемые читатели! Предлагаемый вашему вниманию «Самоучитель по химии» – не обычный учебник. В нем не просто излагаются какие-то факты или описываются свойства веществ. «Самоучитель» объясняет и учит даже в том случае, если вы, к сожалению, не знаете и не понимаете химии, а к учителю обратиться за разъяснениями не можете или стесняетесь. В виде рукописи эта книга используется школьниками с 1991 г., и не было ни одного ученика, который бы провалился на экзамене по химии и в школе, и в вузах. Причем многие из них совсем не знали химии.
«Самоучитель» рассчитан на самостоятельную работу ученика. Главное – отвечать по ходу чтения на те вопросы, которые встречаются в тексте. Если вы не смогли ответить на вопрос, то читайте внимательнее текст еще раз – все ответы имеются рядом. Желательно также выполнять все упражнения, которые встречаются по ходу объяснения нового материала. В этом помогут многочисленные обучающие алгоритмы, которые практически не встречаются в других учебниках. С их помощью вы научитесь:
Составлять химические формулы по валентности;
Составлять уравнения химических реакций, расставлять в них коэффициенты, в том числе в уравнениях окислительно-восстановительных процессов;
Составлять электронные формулы (в том числе краткие электронные формулы) атомов и определять свойства соответствующих химических элементов;
Предсказывать свойства некоторых соединений и определять, возможен данный процесс или нет.
В пособии два уровня сложности. Самоучитель первого уровня сложности состоит из трех частей.
I часть. Элементы общей химии (публикуемая ).
II часть. Элементы неорганической химии.
III часть. Элементы органической химии.
Книг второго уровня сложности тоже три.
Теоретические основы общей химии.
Теоретические основы неорганической химии.
Теоретические основы органической химии.
|
Глава 1. Основные понятия химии.
Глава 2. Важнейшие классы неорганических соединений.
Глава 3. Элементарные сведения о строении атома. Периодический закон Д.И.Менделеева.
Глава 4. Понятие о химической связи. Глава 5. Растворы. Глава 6. Электролитическая диссоциация.
Глава 7. Понятие об окислительно-восстановительных реакциях. Глава 8. Расчеты по химическим формулам и уравнениям.
Приложение. |
Глава 1. Основные понятия химии
Что такое химия? Где мы встречаемся с химическими явлениями?
Химия – везде. Сама жизнь – это бесчисленное множество разнообразных химических реакций, благодаря которым мы дышим, видим голубое небо, ощущаем изумительный запах цветов.
Что изучает химия?
Химия изучает вещества, а также химические процессы, в которых участвуют эти вещества.
Что такое вещество?
Вещество – это то, из чего состоит окружающий нас мир и мы сами.
Что такое химический процесс (явление)?
К химическим явлениям относятся процессы, в результате которых изменяется состав или строение молекул, образующих данное вещество*. Изменились молекулы – изменилось вещество (оно стало другим), изменились его свойства. Например, свежее молоко стало кислым, зеленые листья стали желтыми, сырое мясо при обжаривании изменило запах.
Все эти изменения – следствие сложных и многообразных химических процессов. Однако признаки простых химических реакций, в результате которых изменяется состав и строение молекул, такие же: изменение цвета, вкуса или запаха, выделение газа, света или тепла, появление осадка.
Что же такое молекулы, изменение которых влечет за собой столь разнообразные проявления?
Молекулы – это мельчайшие частицы вещества, отражающие его качественный и количественный состав и его химические свойства.
Изучая состав и строение одной молекулы, можно предсказать многие свойства данного вещества в целом. Такие исследования – одна из главных задач химии.
Как устроены молекулы? Из чего они состоят?
Молекулы состоят из атомов. Атомы в молекуле соединены при помощи химических связей. Каждый атом обозначается при помощи символа (химического знака). Например, Н – атом водорода, О – атом кислорода.
Число атомов в молекуле обозначают при помощи индекса – цифры внизу справа после символа.
Например:
Примеры молекул:
О 2 – это молекула вещества кислорода, состоящая из двух атомов кислорода;
Н 2 О – это молекула вещества воды, состоящая из двух атомов водорода и одного атома кислорода.
Если атомы не связаны химической связью, то их число обозначают при помощи коэффициента – цифры перед символом:

Аналогично изображают число молекул:
2Н 2 – две молекулы водорода;
3Н 2 О – три молекулы воды.
Почему атомы водорода и кислорода имеют разные названия и разные символы? Потому что это атомы разных химических элементов.
Химический элемент – это вид атомов с одинаковым зарядом ядер.
Что такое ядро атома? Почему заряд ядра является признаком принадлежности атома к данному химическому элементу? Чтобы ответить на эти вопросы, следует уточнить: изменяются ли атомы в химических реакциях, из чего состоит атом?
Нейтральный атом не имеет заряда, хотя и состоит из положительно заряженного ядра и отрицательно заряженных электронов:

В ходе химических реакций число электронов любого атома может изменяться, а вот заряд ядра атома не меняется . Поэтому заряд ядра атома – своеобразный «паспорт» химического элемента. Все атомы с зарядом ядра +1 принадлежат химическому элементу под названием водород. Атомы с зарядом ядра +8 относятся к химическому элементу кислороду.
Каждому химическому элементу присвоен химический символ (знак), порядковый номер в таблице Д.И.Менделеева (порядковый номер равен заряду ядра атома), определенное название, а для некоторых химических элементов – особое прочтение символа в химической формуле (табл. 1).
Таблица 1
Символы (знаки) химических элементов
| № п/п | № в таблице Д.И.Менделеева | Символ | Прочтение в формуле | Название |
| 1 | 1 | H | аш | Водород |
| 2 | 6 | C | це | Углерод |
| 3 | 7 | N | эн | Азот |
| 4 | 8 | O | о | Кислород |
| 5 | 9 | F | фтор | Фтор |
| 6 | 11 | Na | натрий | Натрий |
| 7 | 12 | Mg | магний | Магний |
| 8 | 13 | Al | алюминий | Алюминий |
| 9 | 14 | Si | силициум | Кремний |
| 10 | 15 | P | пэ | Фосфор |
| 11 | 16 | S | эс | Сера |
| 12 | 17 | Cl | хлор | Хлор |
| 13 | 19 | K | калий | Калий |
| 14 | 20 | Ca | кальций | Кальций |
| 15 | 23 | V | ванадий | Ванадий |
| 16 | 24 | Cr | хром | Хром |
| 17 | 25 | Mn | марганец | Марганец |
| 18 | 26 | Fe | феррум | Железо |
| 19 | 29 | Cu | купрум | Медь |
| 20 | 30 | Zn | цинк | Цинк |
| 21 | 35 | Br | бром | Бром |
| 22 | 47 | Ag | аргентум | Серебро |
| 23 | 50 | Sn | станнум | Олово |
| 24 | 53 | I | йод | Йод |
| 25 | 56 | Ba | барий | Барий |
| 26 | 79 | Au | аурум | Золото |
| 27 | 80 | Hg | гидраргирум | Ртуть |
| 28 | 82 | Pb | плюмбум | Cвинец |
Вещества бывают простые и сложные . Если молекула состоит из атомов одного химического элемента, это простое вещество. Простые вещества – Са, Сl 2 , О 3 , S 8 и т. д.
Молекулы сложных веществ состоят из атомов разных химических элементов. Сложные вещества – H 2 O, NO, H 3 PO 4, C 12 H 22 O 11 и т. д.
Задание 1.1. Укажите число атомов в молекулах сложных веществ H 2 O, NO, H 3 PO 4 , C 12 H 22 O 11 , назовите эти атомы.
Возникает вопрос: почему для воды всегда записывается формула Н 2 О, а не НО или НО 2 ? Опыт доказывает, что состав воды, полученной любым способом или взятой из любого источника, всегда соответствует формуле Н 2 О (речь идет о чистой воде).
Дело в том, что атомы в молекуле воды и в молекуле любого другого вещества соединены при помощи химических связей. Химическая связь соединяет как минимум два атома. Поэтому, если молекула состоит из двух атомов и один из них образует три химические связи, то другой также образует три химические связи.
Число химических связей , образуемых атомом, называют его валентностью .
Если обозначить каждую химическую связь черточкой, то для молекулы из двух атомов АБ получим АБ, где тремя черточками показаны три связи, образуемые элементами А и Б между собой.
В данной молекуле атомы А и Б трехвалентны.
Известно, что атом кислорода двухвалентен, атом водорода одновалентен.
В о п р о с. Сколько атомов водорода может присоединиться к одному атому кислорода?
О т в е т. Два атома. Состав воды описывают формулой Н–О–Н, или Н 2 О.
П о м н и т е! В устойчивой молекуле не может быть «свободных», «лишних» валентностей. Поэтому для двухэлементной молекулы число химических связей (валентностей) атомов одного элемента равно общему числу химических связей атомов другого элемента.
Валентность атомов некоторых химических элементов постоянна (табл. 2).
Таблица 2
Значение постоянных валентностей некоторых элементов
Для других атомов валентность** можно определить (вычислить) из химической формулы вещества. При этом нужно учитывать изложенное выше правило о химической связи. Например, определим валентность x марганца Mn по формуле вещества MnO 2:
Общее число химических связей, образуемых
одним и другим элементом (Mn и О), одинаково:
x
· 1 = 4; II · 2 = 4. Отсюда х
= 4, т.е. в этой
химической формуле марганец четырехвалентен.
П р а к т и ч е с к и е в ы в о д ы
1. Если один из атомов в молекуле одновалентен, то валентность второго атома равна числу атомов первого элемента (см. на индекс!):
2. Если число атомов в молекуле одинаково, то валентность первого атома равна валентности второго атома:
3. Если у одного из атомов индекс отсутствует, то его валентность равна произведению валентности второго атома на его индекс:
![]()
4. В остальных случаях ставьте валентности «крест-накрест», т.е. валентность одного элемента равна индексу другого элемента:
Задание 1.2. Определите валентности элементов в соединениях:
CO 2 , CO, Mn 2 O 7 , Cl 2 O, P 2 O 3 , AlP, Na 2 S, NH 3 , Mg 3 N 2 .
П о д с к а з к а. Сначала укажите валентность атомов, у которых она постоянная. Аналогично определяется валентность атомных групп ОН, РО 4 , SО 4 и др.
Задание 1.3. Определите валентности атомных групп (в формулах подчеркнуты):
H 3 PO 4 , Ca(OH ) 2 , Ca 3 (PO 4) 2 , H 2 SO 4 , CuSO 4 .
(Обратите внимание! Одинаковые группы атомов имеют одинаковые валентности во всех соединениях.)
Зная валентности атома или группы атомов, можно составить формулу соединения. Для этого пользуются следующими правилами.
Если валентности атомов одинаковы, то и число атомов одинаково, т.е. индексы не ставим:
Если валентности кратны (обе делятся на одно и то же число), то число атомов элемента с меньшей валентностью определяем делением:
В остальных случаях индексы определяют «крест-накрест»:
Задание 1.4. Составьте химические формулы соединений:

Вещества, состав которых отражают химические формулы, могут участвовать в химических процессах (реакциях). Графическая запись, соответствующая данной химической реакции, называется уравнением реакции . Например, при сгорании (взаимодействии с кислородом) угля происходит химическая реакция:
С + O 2 = CO 2 .
Запись показывает, что один атом углерода С, соединяясь с одной молекулой кислорода O 2 , образует одну молекулу углекислого газа СО 2 . Число атомов каждого химического элемента до и после реакции должно быть одинаково . Это правило – следствие закона сохранения массы вещества. Закон сохранения массы: масса исходных веществ равна массе продуктов реакции.
Закон был открыт в XVIII в. М.В.Ломоносовым и, независимо от него, А.Л.Лавуазье.
Выполняя этот закон, необходимо в уравнениях химических реакций расставлять коэффициенты так, чтобы число атомов каждого химического элемента не изменялось в результате реакции. Например, при разложении бертолетовой соли KClO 3 получается соль KСl и кислород О 2:
KClO 3 KСl + О 2 .
Число атомов калия и хлора одинаково, а кислорода – разное. Уравняем их:

Теперь изменилось число атомов калия и хлора до реакции. Уравняем их:
![]()
Наконец, между правой и левой частями уравнения можно поставить знак равенства:
2KClO 3 = 2KСl + 3О 2 .
Полученная запись показывает, что при разложении сложного вещества KClO 3 получаются два новых вещества – сложное KСl и простое – кислород O 2 . Числа перед формулами веществ в уравнениях химических реакций называют коэффициентами .
При подборе коэффициентов необязательно считать отдельные атомы. Если в ходе реакции не изменился состав некоторых атомных групп, то можно учитывать число этих групп, считая их единым целым. Составим уравнение реакции веществ CaCl 2 и Na 3 PO 4:
CaCl 2 + Na 3 PO 4 ……………… .
П о с л е д о в а т е л ь н о с т ь д е й с т в и й
1) Определим валентность исходных атомов и группы PO 4:
![]()
2) Напишем правую часть уравнения (пока без индексов, формулы веществ в скобках надо уточнить):
3) Составим химические формулы полученных веществ по валентностям составных частей:
![]()
4) Обратим внимание на состав самого сложного соединения Ca 3 (PO 4) 2 и уравняем число атомов кальция (их три) и число групп РО 4 (их две):
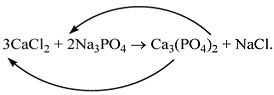
5) Число атомов натрия и хлора до реакции теперь стало равным шести. Поставим соответствующий коэффициент в правую часть схемы перед формулой NaCl:
3CaCl 2 + 2Na 3 PO 4 = Ca 3 (PO 4) 2 + 6NaCl.
Пользуясь такой последовательностью, можно уравнять схемы многих химических реакций (за исключением более сложных окислительно-восстановительных реакций, см. главу 7).
Типы химических реакций. Химические реакции бывают разных типов. Основными являются четыре типа – соединение, разложение, замещение и обмен.
1. Реакции соединения – из двух и более веществ образуется одно вещество:
Например:
Са + Сl 2 = CaCl 2 .
2. Реакции разложения – из одного вещества получаются два вещества или более:
Например:
Ca(HCO 3) 2 CaCO 3 + CO 2 + H 2 O.
3. Реакции замещения – реагируют простое и сложное вещества, образуются также простое и сложное вещества, причем простое вещество замещает часть атомов сложного вещества:
А + ВХ АХ + В.
Например:
Fe + CuSO 4 = Cu + FeSO 4 .
4. Реакции обмена – здесь реагируют два сложных вещества и получаются два сложных вещества. В ходе реакции сложные вещества обмениваются своими составными частями:
Упражнения к главе 1
1. Выучите табл. 1. Проверьте себя, напишите химические символы: серы, цинка, олова, магния, марганца, калия, кальция, свинца, железа и фтора.
2. Напишите символы химических элементов, которые в формулах произносятся как: «аш», «о», «купрум», «эс», «пэ», «гидраргирум», «станнум», «плюмбум», «эн», «феррум», «це», «аргентум». Назовите эти элементы.
3. Укажите число атомов каждого химического элемента в формулах соединений:
Al 2 S 3 , СаS, МnО 2 , NH 3 , Mg 3 P 2 , SO 3 .
4. Определите, какие из веществ – простые, а какие – сложные:
Na 2 O, Na, O 2 , CaCl 2 , Cl 2 .
Прочитайте формулы этих веществ.
5. Выучите табл. 2. Составьте химические формулы веществ по известной валентности элементов и атомных групп:

6. Определите валентность химических элементов в соединениях:
N 2 O, Fe 2 O 3 , PbO 2 , N 2 O 5, HBr, SiH 4 , H 2 S, MnO, Al 2 S 3 .
7. Расставьте коэффициенты и укажите типы химических реакций:
а) Mg + O 2 MgO;
б) Al + CuCl 2 AlCl 3 + Cu;
в) NaNO 3 NaNO 2 + O 2 ;
г) AgNO 3 + BaCl 2 AgCl + Ba(NO 3) 2 ;
д) Al + HCl AlCl 3 + H 2 ;
е) KOH + H 3 PO 4 K 3 PO 4 + H 2 O;
ж) CH 4 C 2 H 2 + H 2 .
* Существуют вещества, построенные не из молекул. Но об этих веществах речь пойдет позже (см. главу 4).
** Строго говоря, по нижеизложенным правилам определяют не валентность, а степень окисления (см. главу 7). Однако во многих соединениях числовые значения этих понятий совпадают, поэтому по формуле вещества можно определять и валентность.
Печатается с продолжением
Глава 1.
Общие химические и экологические закономерности.
С чего начинается химия?
Cложный ли это вопрос? На него каждый ответит по-своему.
В середней школе учащиеся изучают химию в течение ряда лет. Многие довольно хорошо сдают выпускной экзамен по химии. Однако…
Беседы с абитуриентами и затем и студентами первых курсов говорят о том, что остаточные знания по химии после средней школы незначительные. Одни путаются в различных определениях и химических формулах, а другие вообще не могут воспроизвести даже основные понятия и законы химии, не говоря уже о понятиях и законах экологии.
У них химия так и не начиналась.
Химия, по-видимому, начинается с глубокого освоения ее основ, и прежде всего, основных понятий и законов.
1.1. Основные химические понятия.
В таблице Д.И.Менделеева рядом с символом элемента стоят цифры. Одна цифра обозначает порядковый номер элемента, а вторая атомную массу. Порядковый номер имеет свой физический смысл. О нем мы будем вести разговор позже, здесь остановимся на атомной массе и выделим в каких единицах она измеряется.
Следует сразу оговориться, что атомная масса элемента, приведенная в таблице, величина относительная. За единицу относительной величины атомной массы принята 1/12 часть массы атома углерода, изотопа с массовым числом 12, и назвали ее атомной единицей массы /а.е.м./. Следовательно, 1 а.е.м. равна 1/12 части массы изотопа углерода 12 С. И она равна 1,667*10 –27 кг. /Абсолютная масса атома углерода равна 1,99*10 –26 кг./
Атомная масса , приведенная в таблице, является массой атома, выраженной в атомных единицах массы. Величина безразмерная. Конкретно для каждого элемента атомная масса показывает, во сколько раз масса данного атома больше или меньше 1/12 части массы атома углерода.
Аналогичное можно сказать и о молекулярной массе.
Молекулярная масса – это масса молекулы, выраженная в атомных единицах массы. Величина тоже относительная. Молекулярная масса конкретного вещества равна сумме масс атомов всех элементов, входящих в состав молекулы.
Важным понятием химии является понятие «моль». Моль – такое количество вещества, которое содержит 6,02*10 23 структурных единиц /атомов, молекул, ионов, электронов и т.д./. Моль атомов, моль молекул, моль ионов и т.д.
Масса одного моля данного вещества называется его молярной /или мольной/ массой. Она измеряется в г/моль или кг/моль и обозначается буквой «М». Например, молярная масса серной кислоты М Н 2 SO4 =98г/моль.
Следующее понятие «Эквивалент». Эквивалентом /Э/ называют такое весовое количество вещества, которое взаимодействует с одним молем атомов водорода или замещают такое его количество в химических реакциях. Следовательно, эквивалент водорода Э Н равен единице. /Э Н =1/. Эквивалент кислорода Э О равен восьми /Э О =8/.
Различают химический эквивалент элемента и химический эквивалент сложного вещества.
Эквивалент элемента – величина переменная. Она зависит от атомной массы /А/ и валентности /В/, которую элемент имеет в конкретном соединении. Э=А/В. Например, определим эквивалент серы в оксидах SO 2 и SO 3 . В SO 2 Э S =32/4=8, а в SO 3 Э S =32/6=5,33.
Молярную массу эквивалента, выраженную в граммах, называют эквивалентной массой. Следовательно, эквивалентная масса водорода МЭ Н =1г/моль, эквивалентная масса кислорода МЭ О =8г/моль.
Химический эквивалент сложного вещества /кислоты, гидроксида, соли, оксида/– такое количество соответствующего вещества, которое взаимодействует с одним молем атомов водорода, т.е. с одним эквивалентом водорода или замещает такое количество водорода или любого другого вещества в химических реакциях.
Эквивалент кислоты /Э К / равен частному от деления молекулярной массы кислоты на число атомов водорода, участвующих в реакции. Для кислоты H 2 SO 4 , когда оба атома водорода вступают в реакцию H 2 SO 4 +2NaOH=Na 2 SO+2H 2 O эквивалент будет равен Э Н 2 SO4 = М Н 2 SO 4 /n Н =98/2=49
Эквивалент гидроксида /Э гидр. / определяется как частное от деления молекулярной массы гидроксида на число гидроксогрупп, вступающих в реакцию. Например, эквивалент NaOH будет равен: Э NaOH =М NaOH /n ОН =40/1=40.
Эквивалент соли /Э соли / можно рассчитать, поделив ее молекулярную массу на произведение числа атомов металла, вступающих в реакцию, и их валентность. Так, эквивалент соли Al 2 (SO 4) 3 будет равен Э Al 2 (SO 4) 3 =М Al 2 (SO 4) 3 /6=342/2,3=342/6=57.
Эквивалент оксида /Э ок / можно определить, как сумму эквивалентов соответствующих элемента и кислорода. Например, эквивалент СО 2 будет равен сумме эквивалентов углерода и кислорода: Э СО 2 =Э С +Э О =3+8=7.
Для газообразных веществ удобно пользоваться эквивалентными объемами /Э V /. Так как при нормальных условиях моль газа занимает объем 22,4л, то исходя из этой величины, легко определить эквивалентный объем любого газа. Рассмотрим водород. Мольная масса водорода 2г занимает объем 22,4л, тогда его эквивалентная масса 1г занимает объем 11,2л /или 11200мл /. Следовательно Э V Н =11,2л. Эквивалентный объем хлора равен 11,2л /Э VCl =11,2л/. Эквивалентный объем СО равен 3,56 /Э VC О =3,56л/.
Химический эквивалент элемента или сложного вещества используется в стехиометрических расчетах обменных реакций, а в соответствующих расчетах окислительно–восстановительных реакций применяют уже окислительный и восстановительный эквиваленты.
Окислительный эквивалент определяют как частное от деления молекулярной массы окислителя на число электронов, которое он принимает в данной окислително–восстановительной реакции.
Восстановительный эквивалент равен молекулярной массе восстановителя поделенной на число электронов, которое он отдает в данной реакции.
Напишем окислително–восстановительную реакцию и определим эквивалент окислителя и восстановителя:
5N 2 aS+2KMnO 4 +8H 2 SO 4 =S+2MnSO 4 +K 2 SO 4 +5Na 2 SO 4 +8H 2 O
Окислителем в этой реакции является перманганат калия. Эквивалент окислителя будет равен массе KMnO 4 деленной на число электронов, принятых окислителем в реакции (nе=5). Э KMnO 4 =М KMnO 4 /nе=158/5=31,5. Молярная масса эквивалента окислителя KMnO 4 в кислой среде равна 31,5г/моль.
Эквивалент восстановителя Na 2 S будет: Э Na 4 S =М Na 4 S /nе=78/2=39. Молярная масса эквивалента Na 2 S равна 39г/моль.
В электрохимических процессах, в частности при электролизе веществ, пользуются электрохимическим эквивалентом. Электрохимический эквивалент определяют как частное от деления химического эквивалента вещества, выделяемого на электроде, на число Фарадея /F/. Электрохимический эквивалент более подробно будет рассмотрен в соответствующем параграфе курса.
Валентность . При взаимодействии атомов между ними образуется химическая связь. Каждый атом может образовывать только определенное количество связей. Количество связей предопределяет такое уникальное свойство каждого элемента, которое называют валентностью. В наиболее общем виде валентностью называют способность атома образовывать химическую связь. За единицу валентности принимают одну химическую связь, которую способен образовать атом водорода. В связи с этим, водород является одновалентным элементом, а кислород – двухвалентным, т.к. с атомом кислорода могут образовывать связь не более двух водородов.
Умение определять валентность каждого элемента, в том числе и в химическом соединении, является необходимым условием успешного усвоения курса химии.
С валентностью соприкасается и такое понятие химии как степень окисления . Подстепенью окисления понимают тот заряд, который имеет элемент в ионном соединении или имел бы в ковалентном соединении, если бы общая электронная пара бала бы полностью смещена к более электроотрицательному элементу. Степень окисления имеет не только цифровое выражение, но и соответствующий знак заряда (+) или (–). Валентность не имеет этих знаков. Например, в H 2 SO 4 степень окисления: водорода +1, кислорода –2, серы +6, а валентность, соответственно, будет 1, 2, 6.
Валентность и степень окисления в числовых значениях не всегда совпадают по величине. Например, в молекуле этилового спирта СН 3 –СН 2 –ОН валентность углерода 6, водорода 1, кислорода 2, а степень окисления, например, углерода первого –3, второго –1: –3 СН 3 – –1 СН 2 –ОН.
1.2. Основные экологические понятия.
За последнее время понятие “экология” глубоко входит в наше сознание. Это понятие, введенное еще в 1869г Э.Геккелем /происходит от греческого oikos – дом, место, жилище, logos – учение/ все больше и больше тревожит человечество.
В учебниках биологии экологию определяют как науку о взаимоотношениях живых организмов и среды их обитания. Практически созвучное определение экологии дает Б.Небел в своей книге «Наука об окружающей среде» – Экология – наука о различных аспектах взаимодействия организмов между собой и с окружающей средой. В других источниках можно встретить и более широкое толкование. Например, Экология – 1/. Наука, изучающая отношение организмов и их системных совокупностей и окружающей среды; 2/. Совокупность научных дисциплин, исследующих взаимоотношение системных биологических структур /от макромолекул до биосферы/ между собой и с окружающей средой; 3/. Дисциплина, изучающая общие законы функционирования экосистем различного иерархического уровня; 4/. Комплексная наука, исследующая среду обитания живых организмов; 5/. Исследование положения человека как вида в биосфере планеты, его связей с экологическими системами и воздействие на них; 6/. Наука о выживании в окружающей среде. /Н.А.Агиджанян, В.И.Торшик. Экология человека./. Однако под термином «экология» понимают не только экологию как науку, а само состояние окружающей среды и его влияние на человека, животный и растительный мир.
