Алкены строение свойства. Непредельные углеводороды. Алкены. Сравнительная характеристика физических свойств этилена и его гомологов
Физические свойства алкенов похожи на свойства алканов, хотя все они имеют несколько более низкие температуры плавления и кипения, чем соответствующие алканы. Например, пентан имеет температуру кипения 36 °С, а пентен-1 - 30 °С. При обычных условиях алкены С 2 — С 4 - газы. С 5 – С 15 - жидкости, начиная с C 16 - твердые вещества. Алкены не растворимы в воде, хорошо растворимы в органических растворителях.
В природе алкены встречаются редко. Поскольку алкены являются ценным сырьем для промышленного органического синтеза, разработаны многие способы их получения.
1. Основным промышленным источником алкенов служит крекинг алканов, входящих в состав нефти:
3. В лабораторных условиях алкены получают по реакциям отщепления (элиминирования), при которых от соседних атомов углерода отщепляются два атома или две группы атомов, и образуется дополнительная p -связь. К таким реакциям относятся следующие.
1) Дегидратация спиртов происходит при их нагревании с водоотнимающими средствами, например с серной кислотой при температуре выше 150 °С:
При отщеплении Н 2 O от спиртов, НВr и HCl от алкилгалогенидов атом водорода преимущественно отщепляется от того из соседних атомов углерода, который связан с наименьшим числом атомов водорода (от наименее гидрогенизированного атома углерода). Эта закономерность носит название правила Зайцева .
3) Дегалогенирование происходит при нагревании дигалогенидов, имеющих атомы галогена у соседних атомов углерода, с активными металлами:
CH 2 Br —CHBr —CH 3 + Mg → СН 2 =СН-СН 3 + Mg Вr 2 .
Химические свойства алкенов определяются наличием в их молекулах двойной связи. Электронная плотность p -связи достаточно подвижна и легко вступает в реакции с электрофильными частицами. Поэтому многие реакции алкенов протекают по механизму электрофильного присоединения , обозначаемому символом A E (от англ, addition electrophilic ). Реакции злектрофильного присоединения это ионные процессы, протекающие в несколько стадий.
На первой стадии электрофильная частица (чаще всего это бывает протон H +) взаимодействует с p -электронами двойной связи и образует p -комплекс, который затем превращается в карбокатион путем образования ковалентной s -связи между электрофильной частицей и одним из атомов углерода:
алкен p -комплекс карбокатион
На второй стадии карбокатион реагирует с анионом X — , образуя вторую s -связь за счет электронной пары аниона:

Ион водорода в реакциях электрофильного присоединения присоединяется к тому из атомов углерода при двойной связи, на котором больше отрицательный заряд. Распределение зарядов определяется смещением p
-электронной плотности под влиянием заместителей:  .
.
Электронодонорные заместители, проявляющие +I -эффект, смещают p -электронную плотность к более гидрогенизированному атому углерода и создают на нем частичный отрицательный заряд. Этим объясняется правило Марковникова : при присоединении полярных молекул типа НХ(X = Hal , ОН, CN и т.п.) к несимметричным алкенам водород преимущественно присоединяется к более гидрогенизированному атому углерода при двойной связи.
Рассмотрим конкретные примеры реакций присоединения.
1) Гидрогалогенирование . При взаимодействии алкенов с галогеноводородами (HCl , НВr ) образуются алкилгалогениды:
СН 3 -СН=СН 2 + НВr ® СН 3 -СНВr-СН 3 .
Продукты реакции определяются правилом Марковникова.
Следует, однако, подчеркнуть, что в присутствии какого-либо органического пероксида полярные молекулы НХ реагируют с алкенами не по правилу Марковникова:
| R-O-O-R | ||
| СН 3 -СН=СН 2 + НВr | СН 3 -СН 2 -СН 2 Вr |
Это связано с тем, что присутствие перекиси обусловливает радикальный, а не ионный механизм реакции.
2) Гидратация . При взаимодействии алкенов с водой в присутствии минеральных кислот (серной, фосфорной) образуются спирты. Минеральные кислоты выполняют роль катализаторов и являются источниками протонов. Присоединение воды также идет по правилу Марковникова:
СН 3 -СН=СН 2 + НОН ® СН 3 -СН(ОН)-СН 3 .
3) Галогенирование . Алкены обесцвечивают бромную воду:
СН 2 =СН 2 + Вr 2 ® ВrСН 2 -СН 2 Вr.
Эта реакция является качественной на двойную связь.
4) Гидрирование . Присоединение водорода происходит под действием металлических катализаторов:
где R = Н, СН 3 , Cl , С 6 Н 5 и т.д. Молекула CH 2 =CHR называется мономером, полученное соединение - полимером , число n-степень полимеризации.
Полимеризация различных производных алкенов дает ценные промышленные продукты: полиэтилен, полипропилен, поливинилхлорид и другие.
Кроме присоединения, для алкенов характерны также реакции окисления. При мягком окислении алкенов водным раствором перманганата калия (реакция Вагнера ) образуются двухатомные спирты:
ЗСН 2 =СН 2 + 2КМn О 4 + 4Н 2 О ® ЗНОСН 2 -СН 2 ОН + 2MnO 2 ↓ + 2KOH .
В результате протекания этой реакции фиолетовый раствор перманганата калия быстро обесцвечивается и выпадает коричневый осадок оксида марганца (IV ). Эта реакция, как и реакция обесцвечивания бромной воды, является качественной на двойную связь. При жестком окислении алкенов кипящим раствором перманганата калия в кислой среде происходит полный разрыв двойной связи с образованием кетонов, карбоновых кислот или СО 2 , например:
| [О] | ||
| СН 3 -СН=СН-СН 3 | 2СН 3 -СООН |
По продуктам окисления можно установить положение двойной связи в исходном алкене.
Как и все другие углеводороды, алкены горят, и при обильном доступе воздуха образуют диоксид углерода и воду:
С n Н 2 n + Зn /2О 2 ® n СО 2 + n Н 2 О.
При ограниченном доступе воздуха горение алкенов может приводить к образованию монооксида углерода и воды:
С n Н 2n + nО 2 ® nCO + nH 2 O .
Если смешать алкен с кислородом и пропустить эту смесь над нагретым до 200°С серебряным катализатором, то образуется оксид алкена (эпоксиалкан), например:

При любых температурах алкены окисляются озоном (озон более сильный окислитель, чем кислород). Если газообразный озон пропускают через раствор какого-либо алкена в тетрахлор-метане при температурах ниже комнатной, то происходит реакция присоединения, и образуются соответствующие озониды (циклические перекиси). Озониды очень неустойчивы и могут легко взрываться. Поэтому обычно их не выделяют, а сразу после получения разлагают водой - при этом образуются карбонильные соединения (альдегиды или кетоны), строение которых указывает на строение подвергавшегося озонированию алкена.
Низшие алкены - важные исходные вещества для промышленного органического синтеза. Из этилена получают этиловый спирт, полиэтилен, полистирол. Пропен используют для синтеза полипропилена, фенола, ацетона, глицерина.
Для алкенов характерны, прежде всего, реакции присоединения по двойной связи. В основном эти реакции идут по ионному механизму. Пи-связь разрывается, и образуются две новые сигма-связи. Напомню, что для алканов типичными были реакции замещения и шли они по радикальному механизму. Присоединяться к алкенам могут молекулы водорода, эти реакции называются гидрирование, молекулы воды, гидратация, галогены галогенирование, галогенводороды гидрогалогенирование. Но обо всем по порядку.
Реакции присоединения по двойной связи
Итак, первое химическое свойство способность присоединять галогеноводороды, гидрогалогенирование.
Пропен и остальные алкены реагируют с галогеноводородами по правилу Марковникова.

Атом водорода присоединяется к наиболее гидрированному, или правильнее сказать гидрогенизированному, атому углерода.
Вторым номером в нашем списке свойств будет гидратация, присоединение воды.
Реакция проходит при нагревании в присутствии кислоты обычно серной или фосфорной. Присоединение воды происходит также по правилу Марковникова, то есть первичный спирт можно получить только гидратацией этилена, остальные неразветвленные алкены дают вторичные спирты.
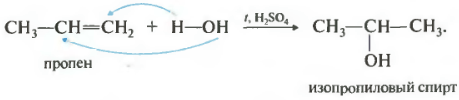
И для гидрогалогениерования и для гидратации существуют исключения из правила Марковникова. Во-первых, против этого правила присоединение протекает в присутствии пероксидов.
Во-вторых, для производных алкенов, в которых присуствуют электронноакцепторне группы. Например, для 3,3,3-трифторпропена-1.

Атомы фтора за счет высокой электроотрицательности оттягивают на себя электронную плотность по цепи сигма-связей. Такое явление называется отрицательным индуктивным эффектом.
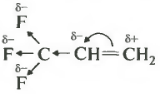
Из-за этого происходит смещение подвижных пи-электронов двойной связи и у крайнего атома углерода оказывается частичный положительный заряд, который обычно обозначается как дельта плюс. Именно к нему и пойдет отрицательно заряженный ион брома, а катион водорода присоединится к наименее гидрированному атому углерода.
Помимо трифторметильной группы отрицательным индуктивным эффектом обладает, например, трихлорметильная группа, нитрогруппа, карбоксильная группа и некоторые другие.
Этот второй случай нарушения правила Марковникова в ЕГЭ встречается очень редко, но все-таки желательно иметь его в виду, если вы планируете сдать экзамен на максимальный балл.
Третье химическое свойство присоединение молекул галогенов.
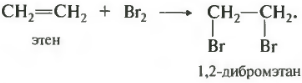
В первую очередь это касается брома, поскольку данная реакция является качественной на кратную связь. При пропускании, например, этилена через бромную воду, то есть раствор брома в воде, имеющий коричневый цвет, происходит ее обесцвечивание. Если пропускать через бромную воду смесь газов, например, этан и этен, то можно получить чистый этан без примеси этена, поскольку тот останется в реакционной колбе в виде дибромэтана, представляющего собой жидкость.
Особым образом стоит отметить реакцию алкенов в газовой фазе при сильном нагревании, например, с хлором.
При таких условиях протекает не реакция присоединения, а реакция замещения. При чем исключительно по альфа-атому углерода, то есть атому, соседствующему с двойной связью. В данном случае получается 3-хлорпропен-1. Эти реакции на экзамене встречаются нечасто, поэтому большинство учеников их не помнит и, как правило, совершает ошибки.
Четвертым номером идет реакция гидрирования, а вместе с ней и реакция дегидрирования. То есть присоединение или отщепление водорода.

Гидрирование происходит при не очень высокой температуре на никелевом катализаторе. При более высокой температуре возможно дегидрирование с получением алкинов.
Пятым свойством алкенов является способность к полимеризации, когда сотни и тысячи молекул алкена за счет разрыва пи-связи и образования сигма-свзяей друг с другом образуют очень длинные и прочные цепочки.
В данном случае получился полиэтилен. Обратите внимание, что в получившейся молекуле кратные связи отсутствуют. Такие вещества называются полимерами, исходные молекулы называются мономерами, повторяющийся фрагмент это элементарное звено полимера, а число n степень полимеризации.
Также возможны реакции получения других важных полимерных материалов, например, полипропилена.
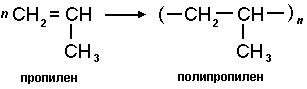
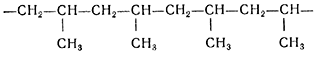
Еще один важный полимер поливинилхлорид.
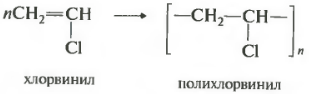
Исходным веществом для производства этого полимера является хлорэтен, тривиальное название которого винилхлорид. Поскольку этот непредельный заместитель называется винил. Часто встречающаяся аббревиатура на пластмассовых изделиях ПВХ как раз расшифровывается как поливинилхлорид.
Мы обсудили пять свойств, которые представляли собой реакции присоединения по двойной связи. Теперь обратимся к реакциям окисления .
Реакции окисления алкенов
Шестое химическое свойство в нашем общем списке это мягкое окисление или реакция Вагнера. Оно протекает при воздействии на алкен водным раствором перманганата калия на холоду, поэтому часто в экзаменационных заданиях указывают температуру ноль градусов.
В результате получается двухатомный спирт. В данном случае этиленгликоль, а в целом такие спирты носят общее название гликоли. В процессе реакции фиолетово-розовый раствор перманганата обесцвечивается, поэтому эта реакция также является качественной на двойную связь. Марганец в нейтральной среде из степени окисления +7 восстанавливается до степени окисления +4. Рассмотрим еще несколько примеров. УРАВНЕНИЕ
Здесь получился пропандиол-1,2. Однако таким же образом будут реагировать и циклические алкены. УРАВНЕНИЕ
Еще один вариант, когда двойная связь находится, например, в боковой цепи ароматических углеводородов. Регулярно в заданиях егэ встречается реакция Вагнера с участием стирола, его второе название винилбензол.
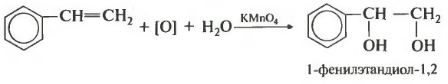
Я надеюсь, что представил вашему вниманию достаточно примеров, чтобы вы поняли, что мягкое окисление двойной связи всегда подчиняется довольно простому правилу пи-связь разрывается и к каждому атому углерода присоединяется гидроксигруппа.
Теперь, что касается жесткого окисления. Это будет наше седьмое свойство. Такое окисление происходит, когда алкен реагирует с кислотным раствором перманганата калия при нагревании.
Происходит деструкция молекулы, то есть ее разрушение по двойной связи. В случае бутена-2 получились две молекулы уксусной кислоты. В целом же, по продуктам окисления можно судить о положении кратной связи в углеродной цепи.
При окислении бутена-1 получается молекула пропионовой (пропановой) кислоты и углекислый газ.
В случае этилена получится две молекулы углекислого газа. Во всех случаях в кислой среде марганец из степени окисления +7 восстанавливается до +2.
И, наконец, восьмое свойство полное окисление или горение.
Алкены сгорают, как и другие углеводороды, до углекислого газа и воды. Запишем уравнение сгорания алкенов в общем виде.
Молекул углекислого газа будет столько же, сколько и атомов углерода в молекуле алкена, поскольку в состав молекулы CO 2 входит один атом углерода. То есть n молекул CO 2 . Молекул воды будет в два раза меньше, чем атомов водорода, то есть 2n/2, а значит просто n.
Атомов кислорода слева и справа одинаковое количество. Справа их 2n из углекислого газа плюс n из воды, итого 3n. Слева атомов кислорода столько же, а значит молекул в два раза меньше, потому как в состав молекулы входят два атома. То есть 3n/2 молекул кислорода. Можно записать 1,5n.
Мы рассмотрели восемь химических свойств алкенов.
Продолжение. Начало см. в № 15, 16, 17, 18, 19/2004
Урок 9.
Химические свойства алкенов
Химические cвойства алкенов (этилена и его
гомологов) во многом определяются наличием в их
молекулах д… связи. Алкены вступают в реакции
всех трех типов, причем наиболее характерными
для них являются реакции п… . Рассмотрим их на
примере пропилена С 3 Н 6 .
Все реакции присоединения протекают по двойной
связи и состоят в расщеплении -связи алкена и образовании на
месте разрыва двух новых -связей.
Присоединение галогенов:

Присоединение водорода (реакция гидрирования):
Присоединение воды (реакция гидратации):

Присоединение галогеноводородов (HHal) и воды к несимметричным алкенам происходит по правилу В.В.Марковникова (1869). Водород кислоты Hhal присоединяется к наиболее гидрированному атому углерода при двойной связи. Соответственно остаток Hal связывается с атомом С, при котором находится меньшее число атомов водорода.

Горение алкенов на воздухе.
При поджигании алкены горят на воздухе:
2СН 2 =СНСН 3 + 9О 2 6СО 2 + 6Н 2 О.
С кислородом воздуха газообразные алкены
образуют взрывчатые смеси.
Алкены окисляются перманганатом калия в водной
среде, что сопровождается обесцвечиванием
раствора KMnO 4 и образованием гликолей
(соединений с двумя гидроксильными группами при
соседних атомах С). Этот процесс – гидроксилирование
алкенов
:

Алкены окисляются кислородом воздуха в эпоксиды при нагревании в присутствии серебряных катализаторов:

Полимеризация алкенов – связывание множества молекул алкена друг с другом. Условия реакции: нагревание, присутствие катализаторов. Соединение молекул происходит путем расщепления внутримолекулярных-cвязей и образования новых межмолекулярных -cвязей:

В этой реакции диапазон значений n = 10 3 –10 4 .
Упражнения.
1. Напишите уравнения реакций бутена-1 с: а) Br 2 ; б) HBr; в) H 2 O; г) H 2 . Назовите продукты реакций.
2.
Известны условия, в которых
присоединение воды и галогеноводородов по
двойной связи алкенов протекает против правила
Марковникова. Составьте уравнения реакций
3-бромпропилена по анти-Марковникову с: а) водой;
б) бромоводородом.
3.
Напишите уравнения реакций
полимеризации: а) бутена-1; б) винилхлорида
СН 2 =СНСl;
в) 1,2-дифторэтилена.
4. Составьте уравнения реакций этилена с кислородом для следующих процессов: а) горение на воздухе; б) гидроксилирование с водным KMnO 4 ; в) эпоксидирование (250 °С, Ag).
5. Напишите структурную формулу алкена, зная, что 0,21 г этого соединения способно присоединить 0,8 г брома.
6. При сгорании 1 л газообразного углеводорода, обесцвечивающего малиновый раствор перманганата калия, расходуется 4,5 л кислорода, причем получается 3 л СО 2 . Составьте структурную формулу этого углеводорода.
Урок 10.
Получение и применение алкенов
Реакции получения алкенов сводятся к обращению
реакций, представляющих химические свойства
алкенов (протеканию их справа налево, см. урок 9).
Надо только подыскать соответствующие условия.
Отщепление двух атомов галогена от
дигалогеноалканов
, содержащих галогены при
соседних атомах С. Реакция протекает под
действием металлов (Zn и др.):

Крекинг предельных углеводородов. Так, при крекинге (см. урок 7) этана образуется смесь этилена и водорода:
Дегидратация спиртов. При действии на спирты водоотнимающих средств (концентрированной серной кислоты) или при нагревании 350 °С в присутствии катализаторов отщепляется вода и образуются алкены:
Таким способом в лаборатории получают этилен.
Промышленным способом получения пропилена
наряду с крекингом служит дегидратация
пропанола над оксидом алюминия:

Дегидрохлорирование хлоралканов проводят при действии на них раствора щелочи в спирте, т.к. в воде продуктами реакции оказываются не алкены, а спирты.
Применение этилена и его гомологов основано на их химических свойствах, т. е. способности превращаться в различные полезные вещества.
Моторные топлива , обладающие высокими октановыми числами, получают гидрированием разветвленных алкенов:

Обесцвечивание желтого раствора брома в инертном растворителе (ССl 4) происходит при добавлении капли алкена или пропускании через раствор газообразного алкена. Взаимодействие с бромом – характерная качественная реакция на двойную связь :
Продукт гидрохлорирования этилена – хлорэтан – используют в химическом синтезе для введения группы С 2 Н 5 – в молекулу:
Хлорэтан также обладает местным анестезирующим (обезболивающим) действием, что используется при хирургических операциях.
Гидратацией алкенов получают спирты, например, этанол :
Спирт C 2 H 5 ОН используют как растворитель, для дезинфекции, в синтезе новых веществ.

Гидратация этилена в присутствии окислителя [O] приводит к этиленгликолю – антифризу и полупродукту химического синтеза :

Окислением этилена получают этиленоксид и ацетальдегид – сырье в химической отрасли промышленности:
![]()
Полимеры и пластики – продукты полимеризации алкенов, например, политетрафторэтилен (тефлон):
Упражнения.
1. Завершите уравнения реакций элиминирования (отщепления), назовите получающиеся алкены :
2.
Составьте уравнения реакций
гидрирования: а) 3,3-диметилбутена-1;
б) 2,3,3-триметилбутена-1. В этих реакциях
получаются алканы, используемые в качестве
моторных топлив, дайте им названия.
3. Через трубку с нагретым оксидом алюминия пропустили 100 г этилового спирта С 2 Н 5 ОН. В результате получили 33,6 л углеводорода (н.у.). Сколько спирта (в %) прореагировало?
4. Сколько граммов брома прореагирует с 2,8 л (н.у.) этилена?
5. Составьте уравнение реакции полимеризации трифторхлорэтилена. (Образующаяся пластмасса устойчива к действию горячей серной кислоты, металлического натрия и т.п.)
Ответы на упражнения к теме 1
Урок 9


5. Реакция алкена С n H 2n с бромом в общем виде:
![]()
Молярная масса алкена M
(С n
H 2n
)
= 0,21 160/0,8 = 42 г/моль.
Это – пропилен.
Ответ
.
Формула алкена – СН 2 =СНСН 3
(пропилен).
6. Поскольку все участвующие в реакции вещества – газы, стехиометрические коэффициенты в уравнении реакции пропорциональны их объемным соотношениями. Запишем уравнение реакции:
С a H в + 4,5О 2 3СО 2 + 3Н 2 О.
Число молекул воды определяем по уравнению
реакции: 4,5 2 = 9 атомов О вступило в реакцию, 6
атомов О связаны в СО 2 , остальные 3 атома О
входят в состав трех молекул Н 2 О. Поэтому
индексы равны: а
= 3, в
= 6. Искомый
углеводород – пропилен С 3 Н 6 .
Ответ
.
Структурная формула
пропилена – СН 2 =СНСН 3 .
Урок 10
1. Уравнения реакций элиминирования (отщепления) – синтез алкенов:

2. Реакции гидрирования алкенов при нагревании под давлением в присутствии катализатора:

3. Реакция дегидратации этилового спирта имеет вид:
![]()
Здесь через х
обозначена масса спирта,
превратившегося в этилен.
Найдем значение х
: х
= 46 33,6/22,4 = 69 г.
Доля прореагировавшего спирта составила: 69/100 =
0,69, или 69%.
Ответ
.
Прореагировало 69% спирта.
4.
![]()
Поскольку стехиометрические коэффициенты
перед формулами реагирующих веществ (С 2 Н 4
и Br 2) равны единице, справедливо
соотношение:
2,8/22,4 = х
/160. Отсюда х
= 20 г Br 2 .
Ответ
.
20 г Br 2 .
Алке́ны (олефины , этиленовые углеводороды C n H 2n
Гомологический ряд.
|
этен (этилен) | |
Простейшим алкеном является этилен (C 2 H 4). По номенклатуре IUPAC названия алкенов образуются от названий соответствующих алканов заменой суффикса «-ан» на «-ен»; положение двойной связи указывается арабской цифрой.
Углеводородные радикалы, образованные от алкенов имеют суффикс «-енил» . Тривиальные названия: CH 2 =CH- «винил» , CH 2 =CH-CH 2 - «аллил» .
Атомы углерода при двойной связи находятся в состоянии sp² гибридизации, и имеют валентный угол 120°.
Для алкенов характерны изомерия углеродного скелета, положения двойной связи, межклассовая и пространственная.
Физические свойства
Температуры плавления и кипения алкенов (упрощенно) увеличиваются с молекулярной массой и длиной главной углеродной цепи.
При нормальных условиях алкены с C 2 H 4 до C 4 H 8 - газы; с пентена C 5 H 10 до гексадецена C 17 H 34 включительно - жидкости, а начиная с октадецена C 18 H 36 - твёрдые вещества. Алкены не растворяются в воде, но хорошо растворяются в органических растворителях.
Дегидрирование алканов
Это один из промышленных способов получения алкенов
Гидрирование алкинов
Частичное гидрирование алкинов требует специальных условий и наличие катализатора
Двойная связь является сочетания сигма- и пи-связей. Сигма- связь возникает при осевом перекрывании sp2 – орбиталей, а пи-связь при боковом перекрывании
Правило Зайцева:
Отщепление атома водорода в реакциях элиминирования происходит преимущественно от наименее гидрогенизированного атома углерода.
13. Алкены. Строение. sp 2 гибридизация, параметры кратной связи. Реакции электрофильного присоединения галогенов, галогеноводородов, хлорноватистой кислоты. Гидратация алкенов. Правило Морковникова. Механизмы реакций.
Алке́ны (олефины , этиленовые углеводороды ) - ациклические непредельные углеводороды, содержащие одну двойную связьмежду атомами углерода, образующие гомологический ряд с общей формулой C n H 2n
Одна s- и 2 p-орбитали смешиваются и образуются 2 равноценные sp2-гибридные орбитали, расположенные в одной плоскости под углом 120.
Если связь образуется более чем одной парой электронов, то она называется кратной .
Кратная связь образуется в тех случаях, когда имеется слишком мало электронов и связывающихся атомов, чтобы каждая пригодная для образования связи валентная орбиталь центрального атома могла перекрыться с какой-либо орбиталью окружающего атома.
Реакции электрофильного присоединения
В данных реакциях атакующей частицей является электрофил.
Галогенирование:
Гидрогалогенирование
Электрофильное присоединение галогенводородов к алкенам происходит по правилу Марковникова
Марковникова правило
Присоединение хлорноватистой кислоты с образованием хлоргидринов:
Гидратация
Реакция присоединения воды к алкенам протекает в присутствии серной кислоты :
Карбкатион - частица, в которой на атоме углерода сосредоточен положительный заряд, атом углерода имеет вакантную p-орбиталь.
14. Этиленовые углеводороды. Химические свойства: реакции с окислителями. Каталитическое окисление, реакция с надкислотами, реакция окисления до гликолей, с разрывом связи углерод-углерод, озонирование. Вакер-процесс. Реакции замещения.
Алке́ны (олефины , этиленовые углеводороды ) - ациклические непредельные углеводороды, содержащие одну двойную связьмежду атомами углерода, образующие гомологический ряд с общей формулой C n H 2n
Окисление
Окисление алкенов может происходить в зависимости от условий и видов окислительных реагентов как с разрывом двойной связи, так и с сохранением углеродного скелета.
При сжигании на воздухе олефины дают углекислый газ и воду.
H 2 C=CH 2 + 3O 2 => 2CO 2 + 2H 2 O
C n H 2n + 3n/O 2 => nCO 2 + nH 2 O – общая формула
Каталитическое окисление
В присутствии солей палладия этилен окисляется до ацетальдегида. Аналогично образуется ацетон из пропена.
При действии на алкены сильных окислителей (KMnO 4 или K 2 Cr 2 O 7 в среде Н 2 SO 4) при нагревании происходит разрыв двойной связи:
При окислении алкенов разбавленным раствором марганцовки образуются двухатомные спирты – гликоли (реакция Е.Е.Вагнера). Реакция протекает на холоде.
Ациклические и циклические алкены при взаимодействии с надкислотами RCOOOH в неполярной, среде образуют эпоксиды (оксираны), поэтому сама реакция носит название реакции эпоксидирования.

Озонирование алкенов.
при взаимодействии алкенов с озоном образуются перекисные соединения, которые называются озо-нидами. Реакция алкенов с озоном является наиболее важным методом окислительного расщепления алкенов по двойной связи
Алкены не вступают в реакции замещения.
Вакер-процесс -процесс получения ацетальдегида прямым окислением этилена.
Вакер-процесс основан на реакции окисления этилена дихлоридом палладия:
CH 2 =CH 2 + PdCl 2 + H 2 O = CH 3 CHO + Pd + 2HCl
15. Алкены: химические свойства. Гидрирование. Правило Лебедева. Изомеризация и олигомеризация алкенов. Радикальная и ионная полимеризация. Понятие полимер, олигомер, мономер, элементарное звено, степень полимеризации. Теломеризация и сополимеризация.
Гидрирование
Гидрирование алкенов непосредственно водородом происходит только в присутствии катализатора. Катализаторами гидрирования служат платина,палладий, никель
Гидрирование можно проводить и в жидкой фазе с гомогенными катализаторами
Реакции изомеризации
При нагревании возможна изомеризация молекул алкенов, которая
может привести как к перемещению двойной связи, так и к изменению скелета
углеводорода.
CH2=CH-CH2-CH3 CH3-CH=CH-CH3
Реакции полимеризации
Это разновидность реакции присоединения. Полимеризация - это реакция последовательного соединения одинаковых молекул в большие по размеру молекулы, без выделения какого-либо низкомолекулярного продукта. При полимеризации атом водорода присоединяется к наиболее гидрогенизированному атому углерода, находящемуся у двойной связи, а к другому атому углерода присоединяется остальная часть молекулы.
CH2=CH2 + CH2=CH2 + ... -CH2-CH2-CH2-CH2- ...
или n CH2=CH2 (-CH2-CH2-)n (полиэтилен)
Вещество, молекулы которого вступают в реакцию полимеризации, называются мономером . Молекула мономера обязательно должна иметь хотя бы одну двойную связь. Образующиеся полимеры состоят из большого количества повторяющихся цепочек, имеющих одинаковое строение (элементарных звеньев). Число, показывающее, сколько раз в полимере повторяется структурное (элементарное) звено, называется степенью полимеризации (n).
В зависимости от вида промежуточных частиц, образующихся при полимеризации, различают 3 механизма полимеризации: а) радикальный; б)катионный; в) анионный.
По первому методу получают полиэтилен высокого давления:
Катализатором реакции выступают пероксиды.
Второй и третий методы предполагает использование в качестве катализаторов кислот (катионная полимеризация), металлорганических соединений.
В химии олигомер ) - молекула в виде цепочки изнебольшого числа одинаковых составных звеньев.
Теломеризация
Теломеризация – олигомеризация алкенов в присутствии веществ – передатчиков цепи (телогенов). В результате реакции образуется смесь олигомеров (теломеров), концевые группы которых представляют собой части телогена. Например, в реакции CCl 4 с этиленом телогеном является CCl 4 .
CCl 4 + nCH 2 =CH 2 => Cl(CH 2 CH 2) n CCl 3
Инициирование этих реакций может осуществляться радикальными инициаторами или g -излучением.
16. Алкены. Реакции радикального присоединения галогенов и галогеноводородов (механизм). Присоединение карбенов к олефинам. Этилен, пропилен, бутилены. Промышленные источники и основные пути использования.
Алкены легко присоединяют галогены, особенно хлор и бром (галогенирование).
Типичной реакцией такого типа является обесцвечивание бромной воды
CH2=CH2 + Вr2 → СH2Br-CH2Br (1,2-дибромэтан)
Электрофильное присоединение галогенводородов к алкенам происходит по правилу Марковникова:
Марковникова правило : при присоединении протонных кислот или воды к несимметричным алкенам или алкинаматом водорода присоединяется к наиболее гидрогенизированному атому углерода
гидрогенизированный атом углерода – тот атом, к которому присоединен водород. Наиболее гидрогенизированный – там где больше всего Н
Реакции присоединения карбенов
Карбены CR 2: - высокореакционные короткоживущие частицы, которые способны легко присоединяться к двойной связи алкенов . В результате реакции присоединения карбена образуются производные циклопропана
Этиле́н - органическое химическое описываемое формулой С 2 H 4 . Является простейшималкеном (олефином )соединение. При нормальных условиях - бесцветный горючий газ со слабым запахом. Частично растворим в воде. Содержит двойную связь и поэтому относится к ненасыщенным или непредельным углеводородам. Играет чрезвычайно важную роль в промышленности. Этилен - самое производимое органическое соединение в мире: Окись этилена; полиэтилен, уксусная кислота, этиловый спирт.
Основные химические свойства (не учи, просто пусть будут на всякий случай, вдруг списать получится)
Этилен - химически активное вещество. Так как в молекуле между атомами углерода имеется двойная связь, то одна из них, менее прочная, легко разрывается, и по месту разрыва связи происходит присоединение, окисление, полимеризация молекул.
Галогенирование:
CH 2 =CH 2 + Br 2 → CH 2 Br-CH 2 Br
Происходит обесцвечивание бромной воды. Это качественная реакция на непредельные соединения.
Гидрирование:
CH 2 =CH 2 + H - H → CH 3 - CH 3 (под действием Ni)
Гидрогалогенирование:
CH 2 =CH 2 + HBr → CH 3 - CH 2 Br
Гидратация:
CH 2 =CH 2 + HOH → CH 3 CH 2 OH (под действием катализатора)
Эту реакцию открыл A.M. Бутлеров, и она используется для промышленного получения этилового спирта.
Окисление:
Этилен легко окисляется. Если этилен пропускать через раствор перманганата калия, то он обесцветится. Эта реакция используется для отличия предельных и непредельных соединений. Окись этилена - непрочное вещество, кислородный мостик разрывается и присоединяется вода, в результате образуетсяэтиленгликоль. Уравнение реакции :
3CH 2 =CH 2 + 2KMnO 4 + 4H 2 O → 3HOH 2 C - CH 2 OH + 2MnO 2 + 2KOH
C 2 H 4 + 3O 2 → 2CO 2 + 2H 2 O
Полимеризация (получение полиэтилена):
nCH 2 =CH 2 → (-CH 2 -CH 2 -) n
Пропиле́н (пропен) СН 2 =СН-СН 3 - непредельный (ненасыщенный) углеводород ряда этилена, горючий газ. Пропилен представляет собой газообразное вещество с низкой температурой кипения t кип = −47,6 °C
Обычно пропилен выделяют из газов нефтепереработки (при крекинге сырой нефти, пиролизе бензиновых фракций) или попутных газов, а также из газов коксования угля.
К непредельным относят углеводороды, содержащие в молекулах кратные связи между атомами углерода. Непредельными являются алкены, алкины, алкадиены (полиены) . Непредельным характером обладают также циклические углеводороды, содержащие двойную связь в цикле (циклоалкены ), а также циклоалканы с небольшим числом атомов углерода в цикле (три или четыре атома). Свойство «непредельности» связано со способностью этих веществ вступать в реакции присоединения, прежде всего водорода, с образованием предельных, или насыщенных углеводородов - алканов.
Строение алкенов
Ациклические углеводороды, содержащие в молекуле помимо одинарных связей, одну двойную связь между атомами углерода и соответствующие общей формуле СnН2n. Свое второе название - олефины
- алкены получили по аналогии с жирными непредельными кислотами (олеиновая, линолевая), остатки которых входят в состав жидких жиров - масел.
Атомы углерода, между которыми есть двойная связь, находятся в состоянии sр 2 -гибридизации. Это означает, что в гибридизации участвуют одна s- и две р-орбитали, а одна р-орбиталь остается негибридизованной. Перекрывание гибридных орбиталей приводит к образованию σ-связи, а за счет негибридизованных р-орбиталей
соседних атомов углерода образуется вторая, π-связь. Таким образом, двойная связь состоит из одной σ- и одной π — связи. Гибридные орбитали атомов, образующих двойную связь, находятся в одной плоскости, а орбитали, образующие π -связь, располагаются перпендикулярно плоскости молекулы. Двойная связь (0,132 им) короче одинарной, а ее энергия больше, т. к. она является более прочной. Тем не менее, наличие подвижной, легко поляризуемой π -связи приводит к тому, что алкены химически более активны, чем алканы, и способны вступать в реакции присоединения.

Строение этилена

Образование двойной связи в алкенах
Гомологический ряд этена
Неразветвленные алкены составляют гомологи- ческий ряд этена (этилена ): С 2 Н 4 - этен, С 3 Н 6 - пропен, С 4 Н 8 - бутен, С 5 Н 10 - пентен, С 6 Н 12 - гексен, С 7 Н 14 - гептен и т.д.
Изомерия алкенов
Для алкенов характерна структурная изомерия. Структурные изомеры отличаются друг от друга строением углеродного скелета. Простейший алкен, для которого характерны структурные изомеры, - это бутен:

Особым видом структурной изомерии является изомерия положения двойной связи:
Алкены изомерны циклоалканам (межклассовая изомерия), например:

Вокруг одинарной углерод-углеродной связи возможно практически свободное вращение атомов углерода, поэтому молекулы алканов могут приобретать самую разнообразную форму. Вращение вокруг двойной связи невозможно, что приводит к появлению у алкенов еще одного вида изомерии - геометрической, или цис- и транс- изомерии .


Цис-изомеры
отличаются от транс-изомеров
пространственным расположением фрагментов молекулы (в данном случае метильных групп) относительно плоскости π -связи, а следовательно, и свойствами.
Номенклатура алкенов
1. Выбор главной цепи.
Образование названия углеводорода начинается с определения главной цепи - самой длинной цепочки атомов углерода в молекуле. В случае алкенов главная цепь должна содержать двойную связь.
2. Нумерация атомов главной цепи.
Нумерация атомов главной цепи начинается с того конца, к которому ближе находится двойная связь.
Например,правильное название соединения:
![]()
Если по положению двойной связи нельзя определить начало нумерации атомов в цепи, то его определяет положение заместителей так же, как для предельных углеводородов.

3. Формирование названия. В конце названия указывают номер атома углерода, у которого начинается двойная связь, и суффикс -ен , обозначающий принадлежность соединения к классу алкенов. Например:

Физические свойства алкенов
Первые три представителя гомологического ряда алкенов - газы; вещества состава С5Н10 — С16Н32 - жидкости; высшие алкены - твердые вещества.
Температуры кипения и плавления закономерно повышаются при увеличении молекулярной массы соединений.
Химические свойства алкенов
Реакции присоединения
. Напомним, что отличительной чертой представителей непредельных углеводородов - алкенов является способность вступать в реакции присоединения. Большинство этих реакций протекает по механизму электрофильного присоединения
.
1. Гидрирование алкенов.
Алкены способны присоединять водород в присутствии катализаторов гидрирования, металлов - платины, палладия, никеля:
Эта реакция протекает при атмосферном и повышенном давлении и не требует высокой температуры, т. к. является экзотермической. При повышении температуры на тех же катализаторах может пойти обратная реакция - дегидрирование.
2. Галогенирование (присоединение галогенов)
. Взаимодействие алкена с бромной водой или раствором брома в органическом растворителе (СС14) приводит к быстрому обесцвечиванию этих растворов в результате присоединения молекулы галогена к алкену и образования дигалогеналканов.
3. Гидрогалогенирование (присоединение галогеноводорода)
.
Эта реакция подчиняется
При присоединении галогеноводорода к алкену водород присоединяется к более гидрированному атому углерода, т. е. атому, при котором находится больше атомов водорода, а галоген - к менее гидрированному.


4. Гидратация (присоединение воды).
Гидратация алкенов приводит к образованию спиртов. Например, присоединение воды к этену лежит в основе одного из промышленных способов получения этилового спирта.
Обратите внимание на то, что первичный спирт (с гидроксогруппой при первичном углероде) образуется только при гидратации этена. При гидратации пропена или других алкенов образуются вторичные спирты .

Эта реакция протекает также в соответствии с правилом Марковникова - катион водорода присоединяется к более гидрированному атому углерода, а гидроксогруппа - к менее гидрированному.
5. Полимеризация.
Особым случаем присоединения является реакция полимеризации алкенов:
Эта реакция присоединения протекает по свободнорадикальному механизму.
Реакции окисления.
1. Горение.
Как и любые органические соединения, алкены горят в кислороде с образованием СО2 и Н2О:
2. Окисление в растворах. В отличие от алканов алкены легко окисляются под действием растворов перманганата калия. В нейтральных или щелочных растворах происходит окисление алкенов до диолов (двухатомных спиртов), причем гидроксильные группы присоединяются к тем атомам, между которыми до окисления существовала двойная связь:




